Artículos médicos
Uso de células madre progenitoras (stem cells) en el tratamiento de enfermedades cardiovasculares:
Futuras proyecciones
Las enfermedades cardiovasculares causan anualmente alrededor de 14 millones de muertes en el mundo. Investigaciones médicas usando terapia con células madre han demostrado resultados prometedores en reparar y regenerar tejido y órganos enfermos. Estos tratamientos conllevan el
inyectar las células madre directamente en el tejido. Las células pueden
entonces regenerarse y convertirse en células nuevas y saludables idénticas a las células del órgano o tejido afectado. Se espera que en un futuro no muy lejano los estudios científicos puedan confirmar y definir los tratamientos empleando estas células.

Juan M. Aranda, MD, FACC
Especialista en Cardiología
Profesor Clínico de Medicina Escuela de Medicina Universidad de Puerto Rico
arandamd@coqui.net
Trasfondo histórico de la terapia con células progenitoras
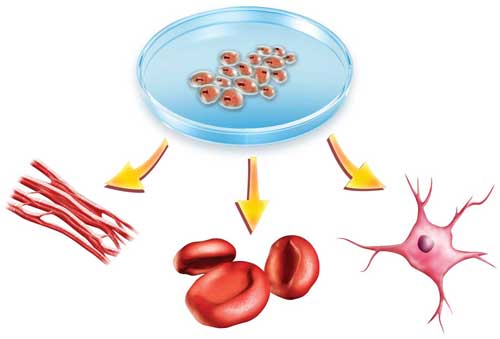
Las células madre o células progenitoras (stem cells) son células maestras pluripotenciales que pueden desarrollarse, diferenciarse y reemplazar a cualquier célula o tejido, sea vascular, cerebral, óseo, intestinal, pancreático y cardiaco, entre otros. Estas observaciones aumentan las posibilidades que los investigadores en biología genética puedan lograr desarrollar tejidos y órganos, por ejemplo para candidatos a transplante cardiaco, o regeneración del cordón espinal en pacientes parapléjicos.
| Las células progenitoras o células madre se pueden dividir (y obtener) en 2 grupos:
1- Células madre embrionarias.
2- Células madre somáticas (o adultas).
Estas últimas se subdividen a su vez en tres subgrupos; las derivadas de la médula ósea, del tejido muscular esquelético y de la sangre periférica. |
Estamos en la era de la revolución geriátrica, en la que las personas entre 65 y 85 años se están cuidando más que los jóvenes, con una disminución en su mortalidad. Esta población ha adquirido lo que se denomina “la plasticidad” del proceso de envejecimiento.
Células madre embrionarias
Las células madre embrionarias están presentes en la capa celular interna del trofoblasto embrionario humano que se desarrolla de la fertilización del óvulo por el espermatozoide. El trofoblasto es la fuente principal de la cual se obtienen las células madre pluripotenciales.
Sin embargo, en el proceso de obtener estas células, se destruye el embrión humano en sus etapas iniciales de desarrollo. Esto último creó una controversia filosófica y moral de tal magnitud, que en el año 2001, en los Estados Unidos las autoridades federales limitaron la disponibilidad de recursos federales para investigación genética usando células madre embrionarias y se prohibió el desarrollo de este tipo de investigación genética. Recientemente el Gobierno Federal levantó la prohibición existente y facilitará la disponibilidad de recursos económicos para el uso de células madre embrionarias para regenerar el tejido específico para pacientes con la enfermedad de Alzheimer, diabetes mellitus y fallo cardiaco congestivo, entre otras condiciones médicas.
Células madre somáticas
Hasta el día de hoy, la investigación clínica se fundamenta en el uso de células madre (células progenitoras) que se obtienen de la médula ósea, de fibras musculares esqueléticas y de la sangre periférica.
Estudios previos reportados en la literatura nos han ayudado a entender el proceso de reparación, regeneración cardiaca y neorevascularización (formación de arterias nuevas). Durante este proceso se requiere la formación o presencia de células endoteliales maduras y nuevas. Estas células nuevas migran de otros tejidos al tejido en reparación o se desarrollan de células progenitoras que se encuentran en la médula ósea (vasculogénesis). Se ha reportado que estas células progenitoras pueden también diferenciarse, desarrollarse y convertirse en células cardiacas (miocitos) nuevas y maduras que ayudan a reparar el tejido cardiaco dañado.
Células madre de médula ósea
Este es el tipo de célula que más se ha utilizado en los estudios de regeneración cardiaca. Se obtienen mediante aspiración de sangre de la médula con anestesia local. El aspirado es centrifugado y filtrado para remover agregados de plaquetas y espículas de hueso. El remanente de células mononucleares, en el que se encuentran las células madre progenitoras, se puede usar directamente en la terapia o puede ser colocado en medios de cultivo especiales para células endoteliales donde pueden crecer, desarrollarse y purificarse. Por medio de este proceso se aumenta el número de células madre disponibles y su efectividad terapéutica. Esto es de suma importancia, ya que existe un número crítico de células madre que tienen que ser inyectadas para que el tratamiento sea efectivo.
El grupo médico del Instituto Cardiaco de Texas fue el primero en utilizar inyecciones de células madre derivadas de la médula ósea; inicialmente en perros y después en pacientes afectados con isquemia del miocardio y disminución en la contractilidad del músculo cardiaco.
Después de administrar las células madre directamente en el músculo cardiaco, inyectándolas en áreas adyacentes a las regiones isquémicas, estudios ecocardiográficos demostraron una mejor contractilidad del músculo cardiaco. Observaciones histopatológicas demostraron que las células madre progenitoras inyectadas se transformaron en células endoteliales (células vasculares) y células cardiacas (miocitos) y regeneraron tejido nuevo.
Células madre de origen muscular esquelético
Estas células se conocen como mioblastos esqueléticos; a través de manipulación genética se convierten en células progenitoras con el aspecto pluripotencial de las células madre embriónicas.
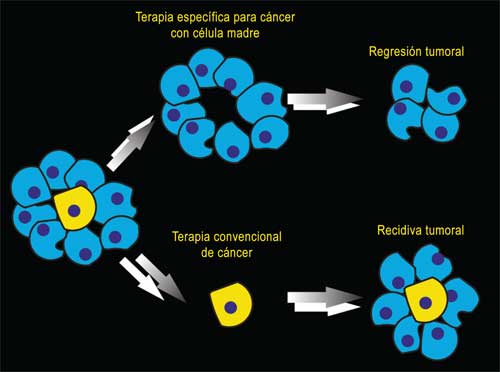
Se obtienen a través de una biopsia de la periferia de un músculo esquelético. El espécimen obtenido se cultiva en medios especiales para obtener células madre que se utilizan para desarrollar y reparar tejido esquelético y óseo. Usando técnicas de manipulación genética se pueden convertir en células madre pluripotenciales con capacidad de diferenciarse a cualquier otro tipo de tejido. Sin embargo, este proceso conlleva al uso de genes cancerosos y las células madre pluripotenciales que se obtienen pueden desarrollar lesiones tumorales al usarse en forma terapéutica. Recientemente se han reportado varios procesos y técnicas para eliminar el riesgo canceroso que conlleva el uso terapéutico de células madre de origen muscular esquelético.
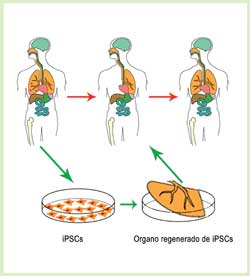
Células madre pluripotenciales inducidas (iPSCs, Induced pluripotent stem cells)
Son células somáticas genéticamente reprogramadas como células madre embrionarias. Las primeras de origen humano fueron reportadas en el año 2007. Cumplen con los criterios de células pluripotenciales y se investiga su grado de semejanza con las células madre de origen embrionario. Estudios recientes confirman que los cardiomiocitos derivados de iPSCs son muy parecidos a los derivados de células madre embrionarias. Esto tiene también una proyección futura muy importante en el campo de trasplantes cardiacos por las limitaciones de órganos existentes.
Células madre pluripotenciales; su seguridad terapéutica
Se ha reportado que la administración intracoronaria de células madre en pacientes con infarto al corazón se asocia a un aumento de reestenosis y trombosis de mallas intracoronarias (stents coronarios). Otros efectos secundarios, cuando se utilizan células, son calcificaciones en el músculo cardiaco y arritmias cardiacas, especialmente cuando se utilizan mioblastos de origen muscular esquelético. Es por esto, que hoy en día para la mayoría de los estudios clínicos se requiere la implantación de un desfibrilador antes de recibir la infusión de células madre directamente al músculo cardiaco.
Conclusiones
La terapia con células madre, células progenitoras pluripotenciales con capacidad de convertirse y diferenciarse a diferentes tipos de células y regenerar vasos sanguíneos, tejido cardiaco, esquelético, cordón espinal, páncreas y otros, está en pleno desarrollo e investigación clínica.
La disponibilidad de células madre humanas de origen embrionario provee una oportunidad única, ya que éstas probablemente son superiores y más efectivas que las células madre somáticas. Las nuevas directrices federales han hecho posible comenzar estudios a largo plazo usando las células madre embrionarias que carecen de los efectos negativos, como los riesgos tumorales, arritmogénicos y las calcificaciones miocárdicas.
Probablemente tendremos disponible dentro de 5 a 10 años los conocimientos y tecnologías necesarias para regenerar todo tipo de tejido anatómico en el cuerpo humano.
Referencias:
1. Circ Res. 2009 Feb 27;104(4):e30-41. Epub 2009 Feb 12, Functional cardiomyocytes derived from human induced pluripotent stem cells. Zhang J, Wilson GF, Soerens AG, Koonce CH, Yu J, Palecek SP, Thomson JA, Kamp TJ.
2. Nature. 2009 Apr 9;458(7239):771-5. Epub 2009 Mar 1. Virus-free induction of pluripotency and subsequent excision of reprogramming factors. Kaji K, Norrby K, Paca A, Mileikovsky M, Mohseni P, Woltjen K.
3. Blood. 2009 Jun 11;113(24):6094-101. Epub 2009 Apr 13. Human embryonic stem cells differentiate into a homogeneous population of natural killer cells with potent in vivo antitumor activity. Woll PS, Grzywacz B, Tian X, Marcus RK, Knorr DA, Verneris MR, Kaufman DS.
4. http://www.isscr.org/public
5. http://www.nlm.nih.gov/medlineplus/stemcells.html