REUMATOLOGÍA
La evaluación y el tratamiento inicial de la artritis reumatoide

Luis M. Vilá, MD
Especialista en Reumatología
Catedrático de Medicina
Director, División de Reumatología Alergia e Inmunología
Programa de Adiestramiento en Reumatología
Recinto de Ciencias Médicas, Universidad de Puerto Rico
Introducción
La artritis reumatoide (AR) es un trastorno autoinmune que se caracteriza por una poliartritis inflamatoria. Esta condición afecta hasta al 1% de la población, y es más frecuente en mujeres y en personas entre los 35 y 50 años. Un diagnóstico y un tratamiento tempranos de la AR pueden evitar consecuencias graves que resulten en daño articular y discapacidad física irreversible. Idealmente, los reumatólogos deben realizar la evaluación y el manejo inicial de la AR. Sin embargo, debido a la escasez de reumatólogos tanto en Puerto Rico como en los Estados Unidos, es probable que el médico primario sea el primero en evaluar a los pacientes con AR hasta que estos logren acceder al reumatólogo. Este escrito está enfocado en los principios básicos de la evaluación y el tratamiento tempranos de la AR que pueden servir de guía para el manejo general del paciente.
La importancia del tratamiento temprano de la artritis reumatoide y los datos en Puerto Rico
El tratamiento subóptimo de la AR se asocia con un mayor riesgo de manifestaciones extraarticulares, discapacidad y mortalidad temprana. En las últimas décadas, ha habido una mayor conciencia del impacto beneficioso de la detección temprana y del tratamiento rápido de la AR con fármacos antirreumáticos modificadores de la enfermedad (FARME), como el metotrexato (MTX), para controlar la enfermedad o retrasar su progresión. No obstante, el marco de tiempo del tratamiento temprano de la AR no se ha definido claramente. Algunos investigadores han definido esta ventana dentro de los 6, 12, o incluso 24 meses posteriores al diagnóstico de la AR.
La definición del Colegio Americano de Reumatología (ACR) de la AR temprana se circunscribe a pacientes con una duración de la enfermedad de menos de 6 meses desde el inicio de los síntomas atribuibles a la AR.1 Utilizando esta definición de la AR temprana, realizamos un estudio en el Recinto de Ciencias Médicas de la Universidad de Puerto Rico para determinar el impacto clínico del tratamiento temprano.2 En una cohorte de 387 puertorriqueños con AR, comparamos los desenlaces clínicos de los pacientes tratados con FARME dentro de los 6 meses desde el inicio de los síntomas con aquellos que recibieron tratamiento tardío (≥ 6 meses). La edad promedio de los pacientes de la cohorte fue de 56.0 años y el 87% fueron mujeres. La duración media del seguimiento fue de 14.9 años. Encontramos que el tratamiento temprano se asoció a una reducción de un 56% de deformidades articulares, un 65% de reemplazo de articulaciones y un 46% de discapacidad a largo plazo. Lo más preocupante de los resultados del estudio fue que solamente el 31.3% de los pacientes recibieron tratamiento temprano, lo que implica que hay que hacer un mayor esfuerzo para lograr que los pacientes con AR tengan un mejor acceso y tratamiento oportuno para prevenir consecuencias serias.
El diagnóstico de la artritis reumatoide
El diagnóstico de la AR se realiza por criterio clínico en un paciente que presenta las características clásicas de la condición, tales como la poliartritis inflamatoria simétrica, la elevación de la velocidad de sedimentación de eritrocitos (ESR) o la proteína C reactiva (CRP), o pruebas positivas de factor reumatoideo (RF) o anticuerpos antipéptidos cíclicos citrulinados. (ACPA).
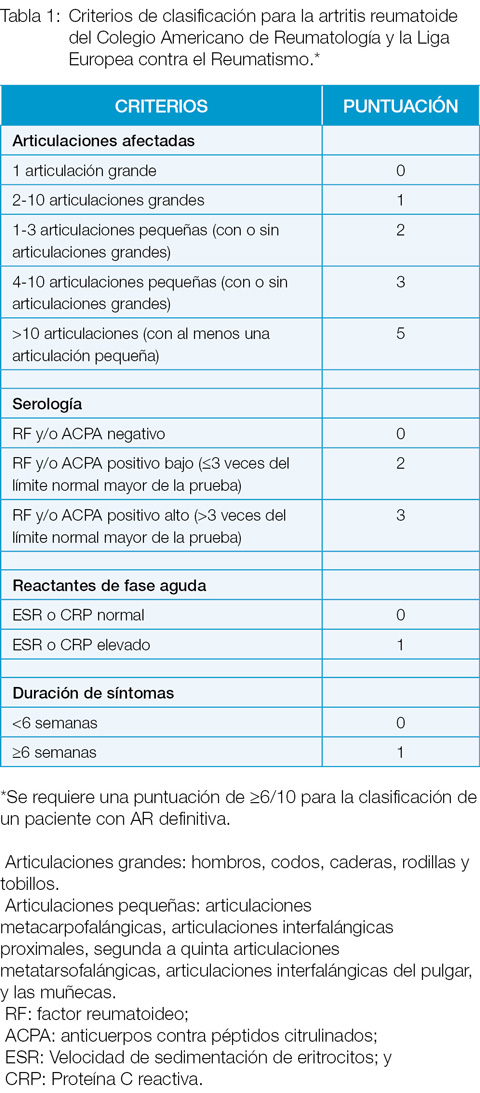
Aunque los criterios clasificatorios de las enfermedades se utilizan principalmente para definir y mantener la uniformidad en los criterios de inclusión de los estudios de investigación, también sirven de guía para hacer los diagnósticos clínicos. La clasificación de la AR establecida en 2010 por el ACR y la Liga Europea contra el Reumatismo (EULAR) (Tabla 1) se dirigió a clasificar a los pacientes con AR de forma más precoz de lo que permitía la clasificación previa.3 Según esta clasificación, un paciente tiene AR si tiene 6 o más puntos. Por otro lado, pacientes con otras condiciones autoinmunes reumáticas tales como el lupus, el síndrome de Sjögren y la artritis psoriásica, la artritis inducida por infecciones virales como parvovirus o virus de chikungunya, y la artritis inducida por cristales pueden causar una artritis inflamatoria similar a la AR, por lo que podrían cumplir erróneamente con estos criterios clasificatorios. Por lo tanto, siempre deben imperar una evaluación completa para descartar estas condiciones y el juicio clínico.
La evaluación inicial
La evaluación inicial del paciente con AR tiene como objetivos determinar el grado de actividad de la condición, la funcionalidad física, la presencia de manifestaciones extraarticulares y los factores asociados a un pobre pronóstico. Por lo tanto, el historial y el examen físico deben ser completos y detallados. Las pruebas de laboratorio deben incluir pruebas de rutina general (conteo sanguíneo completo, análisis de orina y química sanguínea), reactantes de fase aguda (ESR y CRP), serologías de AR (RF y ACPA) y serologías para descartar otras enfermedades reumáticas autoinmunes (niveles de complementos C3 y C4, y anticuerpos antinucleares, anti-dsDNA, anti-Smith, anti-U1RNP, anti-Ro/SSA y anti-La/SSB). En la evaluación de imágenes, al menos deben incluirse radiografías de las manos y de los pies, así como de otras articulaciones que puedan estar afectadas. Idealmente, también se debería realizar sonografía de las articulaciones afectadas pues esta técnica, además de detectar cambios inflamatorios, permite encontrar daño articular más tempranamente que la radiografía convencional. Como los pacientes de AR son tratados con inmunosupresores, la evaluación inicial debe incluir conjuntamente pruebas para detectar la presencia de infecciones crónicas tales como VIH, hepatitis B, hepatitis C y tuberculosis.
Los factores de pobre pronóstico pueden ser determinantes al momento de seleccionar el tratamiento con FARME, por lo que deben considerase tanto en la evaluación inicial como en las visitas subsiguientes. Estos son los siguientes:
- Actividad de la enfermedad persistentemente moderada o alta a pesar de la terapia con FARME convencionales;
- Altos niveles de reactantes de fase aguda;
- Alto número de articulaciones inflamadas;
- Presencia de RF y/o ACPA, especialmente en niveles altos;
- Presencia de erosiones tempranas; y
- Fracaso de 2 o más FARME convencionales.
El tratamiento inicial
Las recomendaciones del tratamiento temprano de la AR están detalladas en las guías establecidas por ACR y EULAR.4-5 En resumen, el objetivo del tratamiento de la AR debe estar dirigido a alcanzar una remisión clínica o una baja actividad de la enfermedad. Si no se ha alcanzado el objetivo a los 6 meses, se debe ajustar la terapia. El MTX debe formar parte de la primera etapa del tratamiento. Este se puede utilizar tanto como monoterapia o en combinación con otros FARME convencionales sintéticos. Generalmente, se comienza en una dosis de 10 a 12.5 mg por vía oral o subcutánea semanal y se va incrementando rápidamente hasta alcanzar una dosis semanal de 20 a 25 mg o de 0.3 mg/kg del peso corporal. En forma concomitante, se administra ácido fólico 1 mg oral diario para prevenir varios de los efectos adversos relacionados con el MTX. En los pacientes con contraindicación al MTX o intolerancia o efectos secundarios tempranos, se puede utilizar la sulfasalazina o la leflunomida. La sulfasalazina se recomienda en una dosis de 3000 mg oral diarios (en dosis dividida, 2 o 3 veces a día) y la leflunomida en una dosis de 20 mg oral diarios. La hidroxicloroquina (200-400 mg diarios) puede utilizarse, pero en pacientes con enfermedad leve que no tengan factores de mal pronóstico. Estos FARME convencionales también pueden utilizarse en combinación con MTX, particularmente en quienes tengan factores de mal pronóstico. Los glucocorticoides en dosis baja (menos de 7.5 mg/día de prednisona o su equivalente) y a corto plazo pueden añadirse a los FARME para controlar la inflamación articular, pero deben suspenderse tan pronto como sea clínicamente posible.
En las mujeres en edad reproductiva hay que tener precaución con el tratamiento de MTX y leflunomida, pues ambos medicamentos pueden causar efectos teratogénicos serios. En la paciente mujer que desee concebir, la sulfasalazina y la hidroxicloroquina serían las opciones más apropiadas pues son seguras tanto en el embarazo como en la lactancia. Por otro lado, las mujeres en edad reproductiva que no tienen planes de embarazo tienen que utilizar métodos anticonceptivos si toman MTX y leflunomida. Por último, en los primeros 6 meses del tratamiento de la AR, generalmente tanto los FARME biológicos como los inhibidores de la quinasa de Janus no se utilizan a menos que el paciente tenga varios factores de mal pronóstico o tengan efectos adversos a los FARME convencionales.
Conclusión
El tratamiento de la AR con FARME dentro de los 6 meses desde el inicio de los síntomas atribuibles a la condición es crucial para reducir el daño físico y el deterioro funcional a largo plazo. Los FARME convencionales sintéticos, en particular el MTX, son recomendados inicialmente. El objetivo de estos fármacos es que el paciente alcance una remisión clínica o baja actividad de la enfermedad en o antes de los 6 meses de tratamiento. Un diagnóstico y un tratamiento oportunos de la AR, al igual que un referido temprano al reumatólogo para el manejo y seguimiento clínico, van a impactar favorablemente en el pronóstico a corto y a largo plazo de los pacientes con esta artritis inflamatoria.
Referencias
- Singh JA, Saag KG, Bridges SL Jr, Akl EA, et al. 2015 American College of Rheumatology Guidelines for the Treatment of Rheumatoid Arthritis. Arthritis Rheumatol. 2016 Jan;68(1):1-26.
- Varela-Rosario N, Arroyo-Ávila M, Fred-Jiménez RM, Díaz-Correa LM, Pérez-Ríos N, Rodríguez N, Ríos G, Vilá LM. Long-term outcomes in Puerto Ricans with rheumatoid arthritis receiving early treatment with disease-modifying anti-rheumatic drugs using the ACR definition of early RA. Open Rheumat J. 2017 Dec;11:136-144.
- Aletaha D, Neogi T, Silman AJ, Funovits J, Felson DT, Bingham CO 3rd, et al. 2010 Rheumatoid arthritis classification criteria: an ACR/EULAR collaborative initiative. Art Rheum. 2010; 62(9):2569-2581.
- Fraenkel L, Bathon JM, England BR, St Clair EW, Arayssi T, Carandang K, et al. 2021 ACR Guideline for the Treatment of Rheum Arthritis. Arthritis Care Res. 2021 Jul;73 (7):924-939.
- Smolen JS, Landewé RBM, Bijlsma JWJ, Burmester GR, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2019 update. Ann Rheum Dis. 2020 Jun;79(6):685-699.








