Resistencia a la hormona tiroidea:
El dilema entre medicar o no medicar

Francisco Nieves Rivera, MD
Endocrinólogo Pediátrico
Catedrático, UPR
Se presenta un varón de 3 años para evaluación por aparente hipotiroidismo central. Según sus padres, el niño fue diagnosticado con perlesía cerebral a los 2 meses de edad y ha estado en seguimiento con múltiples especialistas por retraso global del desarrollo, por problemas de alimentación y por pobre crecimiento. Además, él no habla ni puede caminar. A la edad de 2 años fue diagnosticado con hipotiroidismo central e inició tratamiento con levotiroxina sódica (L-T4). La adherencia al medicamento ha sido excelente. Sin embargo, los niveles de tiroxina libre en sangre permanecen bajos. Se nos consulta para evaluar el fallo de respuesta a la terapia oral con L-T4, en este caso de hipotiroidismo.
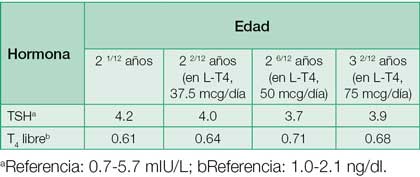
El examen físico demuestra que el niño es pequeño para su edad cronológica: Talla 94.4 cm (-0.23 SD) y peso de 13 kg (-0.95 SD). Sus extremidades muestran espasticidad y movimientos coreoatetoides. No hay tiromegalia. El historial familiar es negativo para disturbios tiroideos; el niño tiene dos hermanas que se encuentran en buen estado de salud. Se sospecha un estado de resistencia a las hormonas tiroideas.
Resistencia a las hormonas tiroideas
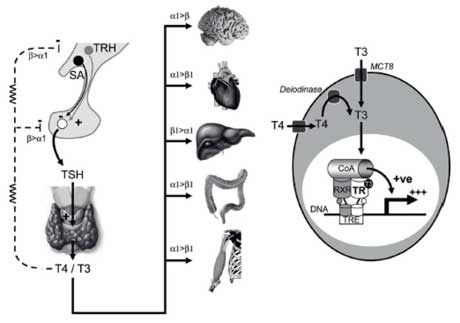
Cualquier proceso que interfiera con la acción de las hormonas tiroideas que incluya defectos en la acción de las hormonas en su transporte o su metabolismo representa un estado de resistencia a estas hormonas (ver figura). El más común de estos defectos se caracteriza por la reducción en la acción intracelular de triyodotironina (T3) que es la hormona tiroidea activa a partir de su precursor: tiroxina o T4. Este defecto fue identificado por primera vez en 1967 como parte de un síndrome de reducción en la respuesta de los tejidos a hormonas tiroideas. Posteriormente, esto se asoció a una mutación del gen que codifica para la porción beta del receptor de hormonas tiroideas. Los defectos de resistencia a hormonas tiroideas se pueden agrupar en:
- Defectos en el transporte de las hormonas tiroideas a nivel de la membrana;
- Defectos en el metabolismo de las hormonas tiroideas; y
- Defectos en acción de las hormonas tiroideas. Entre los defectos en acción de las hormonas tiroideas están los estados de resistencia a las hormonas tiroideas por defectos genéticos del receptor beta de hormona tiroidea y defectos genéticos del receptor alfa de hormona tiroidea.
Mecanismo regulador hormonal tiroideo
El suplido de hormonas tiroideas está asegurado por el mecanismo de control de retroalimentación (feedback) que integra al hipotálamo, a la pituitaria y a la misma glándula tiroides: la disminución en los niveles de hormonas tiroideas estimula la secreción de la hormona liberadora tirotropina (TRH) del hipotálamo y de la hormona estimuladora del tiroides (TSH) de la pituitaria anterior. Esta última estimula a las células foliculares tiroideas a sintetizar y a secretar hormonas tiroideas (T4 y T3). La regulación ulterior en las cantidades de hormonas tiroideas ocurre en el nivel local de acción. Específicamente, la entrada de las hormonas tiroideas a las células está regulada por el transporte activo a nivel de las membranas de las células, activación de T4 por remoción de yodo (5’-deyodinación) para convertirla en T3 o inactivación de T4 y T3 (5-deyodinación) convirtiéndolos en T3 reverso y T2, respectivamente. Por último, la presencia y cantidad de receptores de hormonas tiroideas, a través de los cuales las hormonas tiroideas ejercen su acción, determinan el tipo y grado de respuesta hormonal que se observa.
La acción de las hormonas tiroideas ocurre tanto a nivel del citosol como del núcleo de la célula. Los efectos a este último nivel se conocen como efectos genómicos. Existen dos receptores de hormonas tiroideas (alfa y beta) codificados por genes separados localizados en los cromosomas 17 y 3, respectivamente. Además, diferentes isoformas de receptores se producen a consecuencia de transcripción alterna y splicing (división/empalme). Los receptores tienen estructuras y secuencias similares con regiones para unirse al ADN y a T3. Otras regiones de estos receptores se unen, unos con otros, formando dimerizaciones –homodimerización o heterodimerización– y a otros factores proteínicos cosupresores o coactivadores. En el núcleo los receptores tiroideos actúan como factores de transcripción, regulando la expresión de genes, los cuales son reconocidos por una secuencia específica del ADN (conocidos como elementos-respuestas de hormona tiroidea).
Defectos de resistencia y cuadro clínico
Así que, se debe considerar la posibilidad de un defecto de resistencia a las hormonas tiroideas en todo paciente que presente discordancia en los niveles de hormonas tiroideas y concentraciones de TSH.
Una reducción en los niveles intracelulares de hormona tiroidea puede estar ocasionada por defectos en una o más de las proteínas transportadoras que permiten acceso de la hormona a la célula. De hecho, las proteínas transportadoras defectuosas puede que nunca lleguen a insertarse en la membrana celular y tampoco –por ende– a ejercer su función de mover la hormona circulante al interior de la célula. Un ejemplo de estos defectos es el caso presentado, en el que un defecto en el transportador 8 monocarboxilato (MCT8/SLC16A2) causa un aumento en las concentraciones séricas de T3 y niveles bajos de T4 y T3-reverso, acompañado de déficit psicomotor severo. Este transportador está involucrado en la secreción hormonal por la glándula tiroides. El caso del niño presentado es un ejemplo de este defecto (también conocido como el síndrome de Allan-Hernon-Dudley) que se caracteriza por retardo mental severo ligada al cromosoma X (Xq13.2). Este gen codifica la proteína neuronal MCT8, lo que explica tanto el retardo mental (debido a deficiencia de hormona tiroidea en el sistema nervioso central) y a niveles bajos de T4 libre con niveles normales o altos de TSH. Además, la deficiencia de MCT8 resulta en niveles altos de T3 libre como consecuencia de un aumento en la conversión de T4 a T3 (por lo cual estos últimos tienden a estar elevados). Esto explica por qué la administración exógena de L-T4 tuvo un impacto mínimo en el paciente consultado y por qué estos pacientes no deben recibir reemplazo hormonal de L-T4.
Comentario
Puede haber factores genéticos que alteren el fino mecanismo de control del sistema de hormonas tiroideas, llevando a un cuadro de resistencia a la hormona tiroidea, que se debe de considerar como una posibilidad diagnóstica cuando se encuentran resultados discordantes en los niveles de TSH y T4.
Referencias
- Pediatric Endocrine Self-Assessment Program; 2015-2016.
- Refetoff S, Dumitrescu AM, Weiss RE. Impaired sensitivity to thyroid hormones. UpToDate. Mar 2018.








