Osteoporosis en enfermedad renal

Margarita Ramírez-Vick, MD
Especialista en Endocrinología y Diabetología
La osteoporosis es una condición en la que la fortaleza ósea está comprometida por la disminución en la densidad mineral ósea y por la pobre calidad de los huesos. Consecuencia de esto son las fracturas por fragilidad (espontáneas o causadas por trauma mínimo). Este problema se agudiza en pacientes con insuficiencia renal, ya que la enfermedad crónica renal (ECR) tiene un impacto negativo en la salud ósea. En esta población, la incidencia de fracturas es hasta 4 veces mayor que en la población general, lo que se asocia a una mayor morbimortalidad.1
Patofisiología
Lo que se conoce como osteodistrofia renal suele comprender disturbios en calcio, fosfato, hormona paratiroidea (PTH) y vitamina D. Esto se suele manifestar cuando la tasa de filtración glomerular (GFR) se encuentra por debajo de 60mL/min/1.73m2.
La osteodistrofia renal se clasifica de acuerdo a la tasa de recambio óseo (bone turnover):
- Recambio óseo aumentado, que se manifiesta como hiperparatiroidismo secundario con el desarrollo de osteítis fibrosa quística; y
- Recambio óseo disminuido, que se presenta como enfermedad de hueso adinámico u osteomalacia por deposición de aluminio en el hueso.
Antes de tratar una osteoporosis en la ECR, debemos controlar los disturbios asociados a la osteodistrofia renal. El hiperparatiroidismo que se produce por la hiperfosfatemia –y la consiguiente hipocalcemia– se debe tratar con reemplazo de 25-hidroxivitamina D y captadores de fosfato. Se debe tener en cuenta que los captadores de fosfato basados en calcio pueden ocasionar calcificaciones vasculares y aumentar el riesgo cardiovascular. Al avanzar la insuficiencia renal, disminuye la capacidad de producir la forma activa de vitamina D, aumentando aún más la hipersecreción de PTH. En estos casos, es necesario utilizar calcitriol y análogos de vitamina D o calcimiméticos para controlar el hiperparatiroidismo y disminuir el riesgo de fracturas. Hay que hacer un uso moderado de estos agentes pues en exceso pueden llevar a desarrollar el otro espectro de osteodistrofia renal por recambio óseo disminuido (enfermedad de hueso adinámico).
Síntomas
La enfermedad ósea en ECR suele ser asintomática, pero podría asociarse a debilidad, fracturas, dolor óseo y muscular, y necrosis avascular. El dolor de hueso se ve mayormente en enfermedad adinámica y se debe al recambio óseo disminuido, el cual lleva a una incapacidad de reparar las microfracturas que se producen normalmente con el uso.
Osteoporosis vs. osteodistrofia renal
La osteoporosis puede coexistir con la osteodistrofia renal, pero debemos primero excluir las causas descritas previamente de enfermedad metabólica de hueso asociada a ECR para poder hacer el diagnóstico. La prueba estándar para diagnosticar osteodistrofia renal es la biopsia ósea, pero podemos sospechar de hiperparatiroidismo secundario cuando los niveles de PTH sobrepasan los 500pg/mL y la fosfatasa alcalina sérica está elevada. Por el contrario, en enfermedad adinámica, los niveles de PTH están por debajo de 100pg/mL y la fosfatasa alcalina baja.2
Antes no se recomendaba medir la densidad mineral ósea (BMD) de forma rutinaria en el paciente renal ya que no predice el tipo de osteodistrofia renal que está presente. En las últimas guías –Kidney Disease Improving Global Outcome (KDIGO) de 2017– se han tomado en cuenta estudios prospectivos que han encontrado el valor de medir la BMD para predecir fracturas en el paciente con osteodistrofia renal y/o factores de riesgo para osteoporosis.4
Tratamiento
El tratamiento para la osteoporosis en ECR depende de la anormalidad metabólica que prevalezca, del tipo de enfermedad ósea presente y de la severidad de ECR. Los pacientes con estadios 1 a 3 de ECR con PTH normal y osteoporosis se deben manejar como la población general.3 En estadios 3 a 5 con osteodistrofia renal con BMD baja o fracturas por fragilidad, se debe considerar una biopsia ósea antes de administrar antirresortivos, ya que un hueso adinámico o una osteomalacia no se benefician de estos fármacos.4
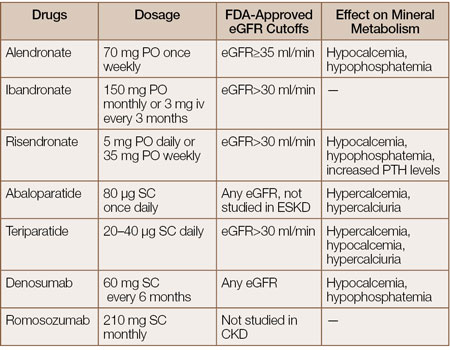
En pacientes con eGFR menor a 35mL/min/1.73m2 está contraindicado el uso de bisfosfonatos, ya que se acumulan en el hueso según disminuye la función renal, causando sobresupresión de la remodelación ósea. Por otro lado, denosumab es un antirresortivo que no se excreta por el riñón, por lo que puede ser administrado en cualquier estadio de ECR, siempre y cuando se evite la hipocalcemia (con suplemento de vitamina D activa antes de la terapia). Los anabólicos se consideran en casos con osteodistrofia renal por recambio óseo disminuido. La teriparatida puede utilizarse con precaución en enfermedad de hueso adinámico, mientras se evite el posible desarrollo de hipercalcemia. Nuevos fármacos anabólicos para osteoporosis, como abaloparatida y romosozumab pudieran ser beneficiosos en pacientes con ECR por el bajo recambio óseo, pero su uso aún se considera off-label por data insuficiente de seguridad –con romosozumab se debe considerar un posible aumento de eventos cardiovasculares, en especial en la población renal–. (Ver Tabla 1).
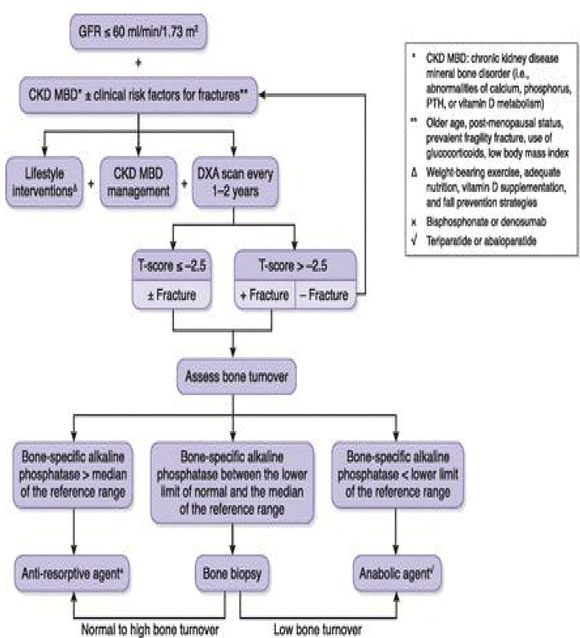
En el siguiente diagrama, podemos ver un algoritmo para decidir las estrategias de manejo en pacientes con ECR y osteoporosis:
Conclusión
El problema de osteoporosis en ECR es prevalente y no debemos dejar de manejarlo por estar la función renal disminuida. Al contrario, debe formar parte del tratamiento holístico que estos pacientes requieren. Aparte de los bisfosfonatos, los demás medicamentos disponibles para osteoporosis –aunque algunos no están aprobados para este uso– podrían ser efectivos en estadios avanzados de insuficiencia renal, sujetos a datos de seguridad.
Referencias
- Alem AM, et al. Increased risk of hip fracture among patients with end-stage renal disease. Kidney Int 2000; 58:396-399.
- Drueke TB, et al. The pathogenesis of parathyroid gland hiperplasia in chronic renal failure. Kidney Int 1995; 48(1):259-272.
- Miller PD, et al. Bone disease in CKD: a focus on osteoporosis diagnosis and management. Am J Kidney Dis 2014; 64(2):290-304.
- Ketteler M, et al. Executive summary of the 2017 KDIGO CKD-MBD guideline update. Kidney Int 2017; 92:26-36.