Endocrinopatías inducidas por inhibidores de puntos de control inmunitario

Michelle Mangual, MD
Endocrinóloga
Directora, Programa de Endocrinología,
Programa de Entrenamiento en Diabetes y Metabolismo
Hospital Municipal, San Juan, Puerto Rico
Los inhibidores de puntos de control inmunitarios (ICI) son una adición importante al arsenal oncológico, y la aplicación de estas terapias para diferentes tipos de cáncer está en constante desarrollo. Los ICI son anticuerpos monoclonales que se pueden utilizar como monoterapia o en combinación. Actúan aprovechando la respuesta inmunológica dirigida a las células malignas mediante el bloqueo de las vías inhibidoras de la regulación de las células T, permitiendo la destrucción de las células cancerosas mediada por las células T. El antígeno de linfocitos T citotóxicos 4 (CTLA-4) y la proteína de muerte celular programada 1 (PD-1) o su ligando (ligando de la proteína de muerte celular programada 1 [PD-L1]) son blanco de los anticuerpos inhibitorios.
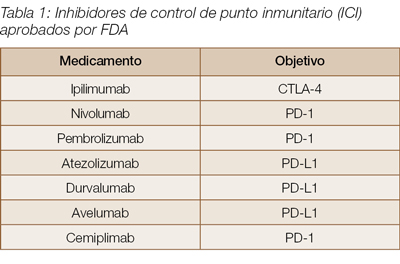
El sistema inmunológico se puede manipular en dos etapas diferentes: CTLA-4 actúa en la etapa inicial de la respuesta antigénica, mientras que PD-1 y PD-L1 actúan para modular las interacciones inmunitarias en los tejidos periféricos (Tabla 1). Por esta razón, la terapia combinada con ambos tipos de agentes se utiliza cada vez más y puede ser más efectiva que cualquier fármaco solo. Sin embargo, estas terapias también pueden ejercer diversos y variables efectos sobre el sistema endocrino provocando reacciones auto inflamatorias contra glándulas endocrinas.
Hipofisitis inducida por los ICI
La inflamación de la glándula pituitaria es el efecto secundario más frecuente y clínicamente importante de ipilimumab relacionado con el sistema endocrino ya que puede llevar a grados significativos de hipopituitarismo. La incidencia global de hipofisitis secundaria al tratamiento con ipilimumab (3 mg/kg) varía del 3% al 17%, dependiendo del estudio y de cómo se definió y registró el evento adverso. Se ha descrito una incidencia mayor al 25% en pacientes con dosis de 10 mg/kg. Además, el riesgo de hipofisitis descrito en los estudios puede ser inexacto debido al retraso en el diagnóstico por el uso simultáneo de glucocorticoides y de quimioterapia para tratar otros eventos adversos relacionados al sistema inmunitario. Se debe destacar que, si las alteraciones hormonales asociadas con ipilimumab no se diagnostican con prontitud, esto puede conducir a una morbilidad significativa e, incluso, a resultados fatales.
Los síntomas clínicos más frecuentes asociados a la hipofisitis inducida por ipilimumab son cefalea y fatiga. Otros incluyen náuseas, anorexia y cambios de presión, que pueden parecerse a los síntomas constitucionales vistos en pacientes con cáncer. Estos síntomas se relacionan con el hecho de que las dos hormonas que se afectan con mayor frecuencia son ACTH y TSH, ya que los corticotropos y los tirotrofos son los 2 tipos más susceptibles de células asociadas con hipofisitis, inducida por ipilimumab.
La incidencia de hipofisitis con anti-PD1 o anti-PD-L1 como monoterapia es inferior a la observada con las terapias anti-CTLA-4. La presentación es diferente, con menos pacientes que reportan cefalea como un síntoma, y solo una pequeña proporción presenta agrandamiento de la hipófisis detectada usando resonancia magnética (28% vs. 98% con ipilimumab).
El tratamiento con anti-PD-1 o anti-PD-L1 tiende a afectar a los corticotrofos de forma aislada, causando insuficiencia adrenal (IA) secundaria. El diagnóstico de IA depende inicialmente de los niveles de cortisol porque la prueba de estimulación con ACTH no es confiable durante la fase aguda. El hipotiroidismo secundario puede mostrar un nivel normal de TSH, por lo que los niveles de T4 libre son más informativos. Aunque la diabetes insípida central inducida por los ICI es rara, se debe considerar de acuerdo a la presentación clínica y llevarnos a sospechar una posible metástasis a la hipófisis. Un MRI para descartar hipofisitis inducida por anti-CTLA-4 puede estar indicado en pacientes con síntomas de efecto de masa local o con diabetes insípida central, mientras que el valor clínico de realizar MRI con el uso de anti-PD-1 o anti-PD-L1 es menos claro debido a la menor probabilidad de agrandamiento de la hipófisis y a la menor incidencia de cefalea como síntoma prevalente.
Disfunción tiroidea inducida por los ICI
Una presentación común, en particular con anti-PD-1 o anti-PDL1, como monoterapia o terapia combinada, es la tiroiditis destructiva con tirotoxicosis transitoria, seguida de hipotiroidismo. También se ha reportado hipotiroidismo de novo y la enfermedad de Graves. Todo paciente en el que se inician los ICI debe someterse a pruebas de función tiroidea, y tener controles en cada ciclo o 4 a 6 semanas desde el inicio de esta terapia, o de acuerdo con los síntomas. El rol de los anticuerpos antitiroideos en la evaluación inicial aún no está claro; sin embargo, pacientes con anticuerpos positivos antes de la terapia ICI tienen mayor riesgo de disfunción tiroidea. Los niveles de inmunoglobulinas estimulantes de TSH, anticuerpos contra el receptor y la tiroglobulina pueden ayudar a distinguir la causa de la tirotoxicosis; en casos en que la fisiopatología no está clara, la sonografía y la captación de yodo radioactivo puede ser útil. En pacientes estables, la tirotoxicosis transitoria se puede tratar con bloqueadores beta.
Diabetes mellitus inducida por los ICI
La terapia ICI puede precipitar la presentación de una deficiencia fulminante de insulina con hiperglucemia severa y cetoacidosis diabética. También puede empeorar el control glucémico en pacientes con diabetes preexistente con terapia oral o con insulina. No hay un rol de la terapia con glucocorticoides en el manejo de diabetes inducida por los ICI. El estado glucémico (glucosa en ayunas y HbA1C) debe evaluarse antes del comienzo de ICI y, los niveles de glucosa, con cada ciclo de ICI. La necesidad de terapia con insulina para la diabetes inducida por ICI es irreversible en la gran mayoría de los casos.
Adrenalitis inducida por los ICI
La IA primaria es más rara en comparación con la IA secundaria, pero es importante distinguir entre los dos tipos para definir la terapia a largo plazo con adición de mineralocorticoides (fludrocortisona). Evaluar los niveles de ACTH, aldosterona y renina puede ser útil en este sentido. La IA primaria puede presentarse como una crisis con inestabilidad hemodinámica y anomalías electrolíticas (hiponatremia e hiperpotase-mia). Un nivel bajo de cortisol matutino (por debajo o en el rango de 3 a 4 mg/dL) puede ser diagnóstico. Un nivel alto de ACTH puede confirmar la naturaleza primaria de la IA (pudiéndose considerar utilizar corticoesteroides) o IA secundaria concomitante si los niveles de ACTH son equívocos. Se debe educar a los pacientes sobre la dosificación del estrés con glucocorticoides y deben usarse dosis más altas para casos agudos (procedimientos u hospitalizaciones).
Conclusión
El éxito de la inmunoterapia en varias formas de cáncer es un adelanto médico significativo. Sin embargo, ha dado lugar a preocupaciones relacionadas a varios efectos del sistema inmunitario sobre las glándulas endocrinas. Como las endocrinopatías figuran entre los efectos adversos más frecuentes, los especialistas deben ser conscientes para poder asegurar un diagnóstico y un manejo temprano y adecuado de estas complicaciones, potencialmente mortales, pero tratables. El cuidado de los pacientes con cáncer incluye la participación de médicos de muchas especialidades: desde médicos de atención primaria hasta de medicina de emergencia. Para todos ellos es importante la comprensión de las endocrinopatías inducidas por los ICI. En muchos pacientes, la función endocrina puede no recuperarse del todo, pero se logrará una supervivencia a largo plazo, incluso con cánceres metastásicos, lo que resultará en un número cada vez mayor de pacientes que requieren reemplazos hormonales de por vida. Ellos requieren cuidado y seguimientos frecuentes por el endocrinólogo como parte del equipo multidisciplinario. Mejorar el conocimiento de las endocrinopatías inducidas por los ICI y su manejo será cada vez más importante en la medida en que la utilización de los ICI siga expandiéndose en el campo oncológico.
Referencias
- Yuen K, et al. AACEndocrinology Disease State Clinical Review: Evaluation and Management of Immune Checkpoint Inhibitor-Mediated Endocrinopathies. Endocrine Practice 28 (2022) 719-731.
- Byun DJ, et al. Cancer immunotherapy immune checkpoint blockade and associated endocrinopathies. Nat Rev Endocr. 2017;13(4):195-207.