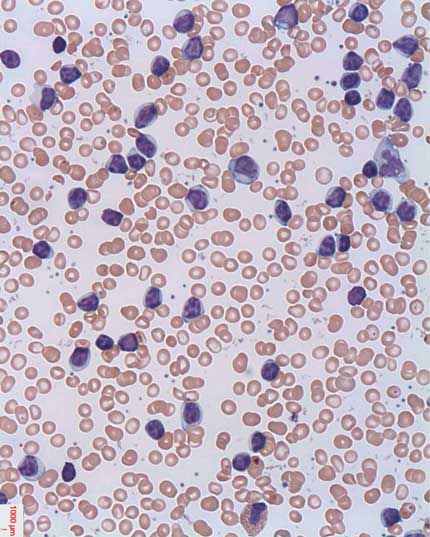
Libres de quimioterapia:
Nuevos tratamientos contra la leucemia linfocítica crónica

Edgardo L. Santiago Guzmán, MD
Hematólogo-Oncólogo
Catedrático Auxiliar, Escuela de Medicina UPR
New Horizons Hematology & Oncology Group
Hospital del Maestro, Suite 2002
Introducción
La leucemia linfocítica crónica (LLC o CLL) es la leucemia más común en adultos, con una incidencia de 5.7 casos por cada 100 000 habitantes al año y representa entre el 30 y el 40% de todas las leucemias. El 90% de los casos se diagnostican en pacientes mayores de 50 años, siendo la edad promedio de diagnóstico entre los 65 y 70 años.
Definición
La LLC es una malignidad clonal de los linfocitos B. Estos presentan marcadores de superficie clásicos de linfocitos maduros, tales como el CD5, CD20 y CD23. Los linfocitos malignos tienen una muerte celular retardada, por lo que se acumulan progresivamente en la sangre periférica, en la médula ósea, en los ganglios linfáticos y en el bazo.
Sintomatología
La gran mayoría de los pacientes se presentan con linfocitosis asintomática, descubierta de manera incidental en hemogramas completos de rutina. Tan solo un 5-10% de los pacientes con LLC presentan síntomas al momento del diagnóstico (los más comunes: fiebre, adenopatías, astenia, pérdida de peso sin razón aparente, dolor abdominal e infecciones frecuentes, como neumonías o herpes zóster).
Diagnóstico
Encontrar más de 5000 linfocitos/mm³ en la sangre periférica puede levantar la sospecha de LLC. La citometría de flujo es la técnica que se utiliza para confirmar el diagnóstico si se logra evidenciar monoclonalidad en los linfocitos.
Cerca del 80% de los pacientes van a presentar anomalías cromosómicas evidenciadas por cariotipo y/o hibridación fluorescente in situ. Las alteraciones más comúnmente encontradas son la del 13q, del 11q, trisomía 12 y la del 17p. La anomalía del 17p afecta a un 10-15% de los pacientes de LLC, caracterizados por la afectación del gen TP53 (gen guardián y supresor de tumores). Estos pacientes suelen tener un peor pronóstico debido a la agresividad de la leucemia y a la capacidad de esta de desarrollar resistencia a los diferentes tratamientos. Por tal razón, la LLC con anomalía del 17p es uno de los focos principales en la investigación clínica.
Tratamiento
No todas las personas requieren ser tratadas al momento del diagnóstico, ya que esta condición suele tener un curso indolente. Algunas de las indicaciones de tratamiento son: anemia, trombocitopenia, linfadenopatía y/o hepatoesplenomegalia sintomática, pérdida de peso de un 10% o más en un periodo de seis meses, fiebre, sudoración nocturna y desórdenes autoinmunes refractarios.
Entre las opciones de tratamiento comúnmente empleadas, se encuentran los siguientes agentes:
Quimioterapia citotóxica: este renglón se divide en los agentes alquilantes (clorambucil, ciclofosfamida y bendamustina) y en los análogos de las purinas (fludarabina, pentostatina y cladribina).
La principal limitación de estos medicamentos es el no poder diferenciar entre las células malignas y las células normales del cuerpo. Por tal razón, el perfil de toxicidad es más amplio y los eventos adversos más comúnmente observados son: náuseas, vómitos, diarreas, caída de cabello y disminución en el número de glóbulos blancos, de hemoglobina y de plaquetas, entre otros. La quimioterapia citotóxica sigue siendo muy efectiva y es mayormente utilizada en combinación con otros agentes en pacientes menores de 65 años sin anomalías genéticas relacionadas al cromosoma 17.
Anticuerpos monoclonales anti-CD20: son medicamentos intravenosos que actúan uniéndose a la proteína CD20 expresada en la membrana de las células B, causando la eliminación de esta célula mediante la activación de complemento, formación de anticuerpos y apoptosis.
Los medicamentos principales en este grupo son rituximab, ofatumumab y obinutuzumab. Cada uno de ellos tiene una afinidad diferente al CD20. En un ensayo clínico, el rituximab en combinación con el clorambucil demostró una reducción estadísticamente significativa de un 61% en la supervivencia libre de progresión versus el clorambucil en monoterapia. De la misma manera, las tasas de respuestas completas y la supervivencia global fueron estadísticamente superiores en el brazo de la combinación. Con estos resultados tan alentadores, la combinación de rituximab con otros agentes citotóxicos marcó el inicio de una nueva era en el tratamiento de los desórdenes linfoproliferativos en general.
El estudio CLL11 comparó el obinutuzumab o rituximab en combinación con clorambucil. Los resultados demostraron que la combinación con obinutuzumab fue superior al disminuir el riesgo de progresión en un 51% y el riesgo de muerte en un 24% en comparación con rituximab más clorambucil.
En base a la efectividad reportada, las guías establecen que la combinación de un anti-CD20 con clorambucil se debe considerar como tratamiento de primeria línea en pacientes frágiles y mayores de 65 años sin alteración del 17p.
Terapia dirigida a una diana molecular: en este grupo se encuentran ibrutinib, idelalisib y venetoclax.
El ibrutinib es un medicamento oral que bloquea la proteína quinasa de Bruton (BTK), caracterizada por ser crucial para la proliferación celular. El estudio RESONATE-2 comparó la eficacia de ibrutinib versus clorambucil en pacientes mayores de 65 años que no habían recibido terapias previas. El ibrutinib disminuyó significativamente el riesgo de progresión y muerte en un 84%. Las tasas de respuestas objetivas también fueron estadísticamente superiores en el grupo de ibrutinib (86% versus 35%, p<0.001). En otros estudios clínicos, el ibrutininb también demostró ser efectivo en pacientes previamente tratados con o sin alteraciones en el cromosoma 17. Con estos resultados nunca antes vistos, en febrero de 2014 se le otorgó la aprobación al ibrutinib en primera o segunda línea de tratamiento para pacientes con LLC, independiente de alteración del 17p.El idelalisib es otro agente oral que bloquea una quinasa diferente (PI3K-δ). Este medicamento recibió aprobación en julio de 2014, en monoterapia y en combinación con rituximab en pacientes que habían progresado a tratamientos previos, incluyendo aquellos con alteración del 17p.El venetoclax es un inhibidor selectivo de la proteína antiapoptótica BCL-2. La expresión de esta proteína está asociada a un aumento en la supervivencia de las células tumorales y a su resistencia a diferentes medicamentos. Su aprobación está fundamentada en el estudio MURANO, donde se comparó la combinación de venetoclax con rituximab versus bendamustina con rituximab en pacientes con LLC que habían recibido al menos una línea de terapia previamente. La tasa de respuesta objetiva fue del 92% en el brazo de venetoclax con rituximab en comparación con un 72% para los tratados con bendamustina más rituximab. En junio de 2018, el venetoclax en combinación con el rituximab, recibió la aprobación para pacientes con LLC -con o sin alteración de 17p- que hayan recibido al menos una terapia previa.Estos agentes modernos son mejor tolerados que la quimioterapia tradicional, ya que actúan en un lugar específico de la célula maligna y, en general, no tienen ningún efecto sobre las células normales del cuerpo.
Comentario
Por la pasada década, la combinación de un anticuerpo monoclonal anti-CD20 (rituximab, ofatumumab, obinutuzumab) con la quimioterapia citotóxica (fludarabina, ciclofosfamida, clorambucil) representaba la terapia de elección para todos los pacientes con LLC.
El descubrimiento de las terapias dirigidas a una diana molecular (ibrutinib, idelalisib, venetoclax) sin duda alguna ha revolucionado el tratamiento de la LLC demostrando en estudios clínicos un aumento estadísticamente significativo en las tasas de respuestas objetivas, supervivencia libre de progresión y supervivencia global en todos los pacientes de LLC –incluyendo aquellos con alteraciones cromosómicas de alto riesgo–.
El descubrimiento de estos medicamentos ha dejado varias preguntas en el tintero, ya que, a pesar de haberse logrado un enorme avance en el manejo de esta condición, aún está por descubrirse cuál es la combinación perfecta para lograr su cura.