ONCOLOGÍA
Pruebas genéticas en pacientes concáncer de seno:
Herramientas de diagnóstico y estrategias terapéuticas para el manejo de mutaciones genéticas

Catedrática Asociada
Escuela de Medicina
Centro Comprensivo de Cáncer
Universidad de Puerto Rico
Epidemiología del cáncer de seno en Puerto Rico
El cáncer de seno es la malignidad más común en las mujeres puertorriqueñas. Los datos del Registro Central de Cáncer de Puerto Rico indican que anualmente se diagnostican cerca de 2,242 casos de cáncer de seno1. De estos, alrededor de 18 casos se encuentran en hombres.2
Pruebas genéticas y cáncer de seno

Las pruebas genéticas tienen el propósito de identificar mutaciones que pudieran aumentar el riesgo de desarrollarciertos tipos de cáncer. La presencia de estas mutaciones da paso a recomendaciones de intervenciones profilácticas para disminuir el riesgo de desarrollar un cáncer. Además, pueden tener implicaciones terapéuticas, ya que la presencia de ciertas mutaciones permite la utilización de algunas terapias dirigidas para el tratamiento del cáncer.
Por otro lado, las pruebas genéticas podrían tener también implicaciones para los familiares del paciente que tiene la mutación, pues dependiendo del patrón de herencia, dichas mutaciones se pueden encontrar en familiares antes de que desarrollen el cáncer y, por ende, se podrían realizar intervenciones preventivas para minimizar o eliminar el desarrollo de estas malignidades.
Guías recientes para pruebas genéticas en el cáncer de seno
En los últimos años, ha habido una proliferación de paneles de pruebas genéticas. A principios de este año, la Sociedad Americana de Oncología Clínica y la Sociedad de Cirugía Oncológica publicaron unas guías sobre el uso de pruebas genéticas en pacientes con cáncer de seno.3
En dichas guías, se recomienda realizar pruebas para identificar mutaciones de BRCA1/2 en todos los pacientes con diagnóstico de cáncer de seno que sean menores de 65 años. En pacientes con cáncer de seno localizado, la presencia de mutaciones de BRCA1/2 puede cambiar el manejo quirúrgico, ya que podría considerarse una mastectomía bilateral en lugar de lumpectomías en pacientes sin mutación.
Tratamientos personalizados para mutaciones BRCA en cáncer de seno
Alrededor del 5% al 9.7% de las pacientes con cáncer de seno metastásico tienen mutaciones de BRCA1/2.4 Estas pacientes pueden beneficiarse del uso de medicamentos inhibidores de la proteína PARP (poly ADP ribose polymerase). En el estudio OlympiAD, se comparó el uso de olaparib, un inhibidor de PARP, con quimioterapia convencional en pacientes de cáncer de seno positivo a receptores hormonales, pero negativo a amplificación de la proteína Her-2/neu, que tuvieran la mutación de BRCA1/2.5 La sobrevida libre de enfermedad fue mayor en el grupo de los pacientes que recibieron olaparib (7 meses frente a 4.2 meses). Aunque no se detectaron diferencias en la sobrevida global, el riesgo de progresión de la enfermedad o muerte fue un 42% menor en el grupo de pacientes que recibió olaparib. En enero de 2018, se aprobó el uso de este medicamento para pacientes con cáncer de seno metastásico con mutaciones BRCA1/2. Otro inhibidor de la proteína PARP, talazoparib, fue aprobado por la FDA desde octubre de 2018 para pacientes con la mutación BRCA1/2 cuyo cáncer de seno sea localmente avanzado o metastásico.
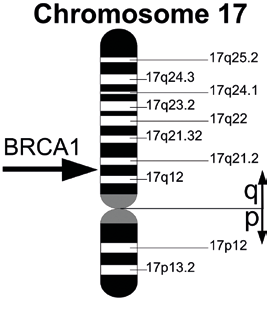
de mama tipo 1
Ubicación del gen BRCA1
en el cromosoma 17
El uso de estos inhibidores de la proteína PARP no es exclusivo para pacientes con enfermedad metastásica. El estudio OlimpiA incluyó a pacientes con cáncer de seno localizado, no metastásico, y con mutación de BRCA1/2. En el estudio, los pacientes fueron aleatorizados para recibir olaparib o placebo durante un año tras completar su tratamiento de quimioterapia y/o cirugía.6 El estudio demostró que la sobrevida libre de enfermedad a tres años era mayor en el grupo que recibió olaparib (85.9% frente al 77.1%). En marzo de 2022, se aprobó el uso de olaparib en el escenario adyuvante en pacientes con cáncer de seno no metastásico y con mutación de BRCA1/2.
En pacientes mayores de 65 años, se recomienda realizar pruebas de BRCA1/2 en aquellos que sean candidatos al uso de inhibidores de PARP, en pacientes con diagnóstico de cáncer de seno triple negativo, en aquellos con historial familiar sugestivo de estas mutaciones, en hombres con diagnóstico de cáncer de seno y en pacientes de ascendencia judía asquenazi.
Mutaciones adicionales y síndromes genéticos asociados
Existen otras mutaciones y síndromes genéticos en pacientes con cáncer de seno, aunque su prevalencia es menor. Las guías de la Sociedad Americana de Oncología Clínica recomiendan pruebas para mutaciones en los genes PALB2, CDH1, PTEN, STK11 y TP53. Identificar estas mutaciones y los síndromes relacionadas con estas permite ofrecer intervenciones terapéuticas antes del desarrollo del cáncer y/o ofrecer al paciente programas de cribado o de diagnóstico desde una edad temprana.
- Por ejemplo, los pacientes con mutaciones de PALB2 tienen un riesgo mayor de desarrollar cáncer de páncreas y ovario,8 por lo que deben ser referidos a un consejero genético con el fin de desarrollar un programa de vigilancia o cribado de estas malignidades;
- Los pacientes con mutaciones en CDH1, además de tener un riesgo aumentado de carcinoma lobular de seno, pueden padecer de cáncer gástrico difuso hereditario y considerar una gastrectomía para minimizar el riesgo de desarrollar cáncer de estómago;9
- Los pacientes con mutaciones en PTEN pueden desarrollar hamartomas y cáncer de seno, de tiroides, de riñón y otros.10 Por ello, deben participar de programas de cribado para estas malignidades;
- Las mutaciones de STK11 se asocian al síndrome de Peutz-Jeghers. Los pacientes que padecen este último pueden desarrollar pólipos gastrointestinales y varios cánceres ginecológicos (de ovario, de cuello uterino, de útero), de testículo, de seno, de colon, de estómago, de intestino delgado, de páncreas y de pulmón; y 11
- Las mutaciones de TP53 están vinculadas con el síndrome de Li-Fraumeni, aumentando el riesgo de desarrollar sarcomas de tejido blando, osteosarcomas, cánceres de glándula adrenal y del sistema nervioso central, y cáncer de seno antes de los 30 años.12
Reacción de los pacientes ante diagnósticos de riesgo genético aumentado
Desde la perspectiva de los pacientes, la posibilidad de ser diagnosticados con cáncer de seno y con mutaciones que predisponen a varios tipos de cáncer puede generar ansiedad e incluso depresión. Sin embargo, estudios indican que los pacientes con diagnósticos de cáncer hereditario suelen estar interesados en conocer más sobre su condición y, en muchos casos, adoptan estilos de vida saludables y un sentido de control, ya que en ocasiones pueden participar de intervenciones preventivas.
Por otro lado, identificar a pacientes con síndromes genéticos permite realizar diagnósticos tempranos y ofrecer intervenciones a sus familiares, quienes también pueden beneficiarse de estas medidas preventivas.
Comentario
En todo paciente con diagnóstico de cáncer de seno, las pruebas de cribado para síndromes genéticos deben ser consideradas como una parte integral de su evaluación. La recopilación de un historial familiar detallado, que incluya edades y tipos de diagnósticos oncológicos, es fundamental para guiar estrategias terapéuticas óptimas para el paciente. Además, estos estudios permiten un diagnóstico temprano y la intervención en familiares que podrían estar en riesgo, ofreciendo un enfoque preventivo que extiende los beneficios de un diagnóstico y del manejo clínico adecuado a toda la familia.
Referencias
- Torres-Cintrón CR, Suárez-Ramos, T, Román-Ruiz Y, Ortiz-Ortiz KJ, De Jesús-Monge V, Gierbolini Bermúdez A, Zavala-Zegarra D, Tortolero-Luna G (2023). Cáncer en Puerto Rico, 2016-2020. Registro Central de Cáncer de Puerto Rico. San Juan, PR.
- https://rcpr.org/Datos-de-C%C3%A1ncer/Tasas-y-Mapas
- Bedrosian I, Somerfield MR, Achatz MI, Boughey JC, et al. Germline Testing in Patients with Breast Cancer: ASCO-Society of Surgical Oncology Guideline. J Clin Oncol. 2024 Feb 10;42(5):584-604.
- O’Shaughnessy J, Brezden-Masley C, Cazzaniga M, et al. Prevalence of germline BRCA mutations in HER2-negative metastatic breast cancer: global results from the real-world, observational BREAKOUT study. Breast Cancer Res. 2020 Oct 27;22(1):114.
- Robson M, Im SA, Senkus E, Xu B, Domchek SM, Masuda N, et al. Olaparib for Metastatic Breast Cancer in Patients with a Germline BRCA Mutation. N Engl J Med. 2017 Aug 10;377(6):523-533. doi: 10.1056/NEJMoa1706450. Epub 2017 Jun 4. Erratum in: N Engl J Med. 2017 Oct 26;377(17):1700.
- Tutt ANJ, Garber JE, Kaufman B, Viale G, Fumagalli D, et al. A Clinical Trial Steering Committee and Investigators. Adjuvant Olaparib for Patients with BRCA1- or BRCA2-Mutated Breast Cancer. N Engl J Med. 2021 Jun 24;384(25):2394-2405. doi: 10.1056/NEJMoa2105215. Epub 2021 Jun 3. PMID: 34081848; PMCID: PMC9126186
- Tung N, Ricker C, Messersmith H, Balmaña J, et al. Selection of Germline Genetic Testing Panels in Patients With Cancer: ASCO Guideline. J Clin Oncol. 2024 Jul 20;42(21):2599-2615.
- Tan MH, Mester JL, Ngeow J, Rybicki LA, Orloff MS, Eng C. Lifetime cancer risks in individuals with germline PTEN mutations. Clin Cancer Res. 2012 Jan 15;18(2):400-7.
- Luo W, Fedda F, Lynch P, Tan D. CDH1 Gene and Hereditary Diffuse Gastric Cancer Syndrome: Molecular and Histological Alterations and Implications for Diagnosis And Treatment. Front Pharmacol. 2018 Dec 5;9:1421.
- Tischkowitz M, Colas C, Pouwels S, Hoogerbrugge N; PHTS Guideline Development Group; European Reference Network GENTURIS. Cancer Surveillance Guideline for individuals with PTEN hamartoma tumour syndrome. Eur J Hum Genet. 2020 Oct;28(10):1387-1393.
- Krishnamurthy N, Goodman AM, Barkauskas DA, Kurzrock R. STK11 alterations in the pan-cancer setting: prognostic and therapeutic implications. Eur J Cancer. 2021 May;148:215-229.
- Frebourg T, Bajalica Lagercrantz S, Oliveira C, Magenheim R, Evans DG; European Reference Network GENTURIS. Guidelines for the Li-Fraumeni and heritable TP53-related cancer syndromes. Eur J Hum Genet. 2020 Oct;28(10):1379-1386.





















